Sकॅन्डियम, ज्याचे घटक चिन्ह Sc आणि अणुक्रमांक २१ आहे, ते पाण्यात सहज विरघळते, गरम पाण्याशी संवाद साधू शकते आणि हवेत सहजपणे गडद होते. त्याची मुख्य संयुजा +3 आहे. ते बहुतेकदा गॅडोलिनियम, एर्बियम आणि इतर घटकांसह मिसळले जाते, ज्याचे उत्पादन कमी असते आणि कवचात अंदाजे 0.0005% असते. स्कॅन्डियमचा वापर अनेकदा विशेष काच आणि हलके उच्च-तापमान मिश्रधातू बनवण्यासाठी केला जातो.
सध्या, जगात स्कॅन्डियमचे सिद्ध साठे फक्त 2 दशलक्ष टन आहेत, त्यापैकी 90-95% बॉक्साइट, फॉस्फोराइट आणि लोह टायटॅनियम धातूंमध्ये आणि एक छोटासा भाग युरेनियम, थोरियम, टंगस्टन आणि दुर्मिळ पृथ्वी धातूंमध्ये आढळतो, जे प्रामुख्याने रशिया, चीन, ताजिकिस्तान, मादागास्कर, नॉर्वे आणि इतर देशांमध्ये वितरित केले जातात. चीन स्कॅन्डियम संसाधनांमध्ये खूप समृद्ध आहे, ज्यामध्ये स्कॅन्डियमशी संबंधित प्रचंड खनिज साठे आहेत. अपूर्ण आकडेवारीनुसार, चीनमध्ये स्कॅन्डियमचे साठे सुमारे 600000 टन आहेत, जे बॉक्साइट आणि फॉस्फोराइट साठ्यांमध्ये, दक्षिण चीनमध्ये पोर्फीरी आणि क्वार्ट्ज व्हेन टंगस्टन साठ्यांमध्ये, दक्षिण चीनमध्ये दुर्मिळ पृथ्वी साठ्यांमध्ये, आतील मंगोलियामध्ये बायान ओबो दुर्मिळ पृथ्वी लोह धातू साठ्यामध्ये आणि सिचुआनमध्ये पंझिहुआ व्हॅनेडियम टायटॅनियम मॅग्नेटाइट साठ्यामध्ये आढळतात.
स्कॅन्डियमच्या कमतरतेमुळे, स्कॅन्डियमची किंमत देखील खूप जास्त आहे आणि त्याच्या शिखरावर, स्कॅन्डियमची किंमत सोन्याच्या किमतीच्या १० पटीने वाढली होती. स्कॅन्डियमची किंमत कमी झाली असली तरी, ती अजूनही सोन्याच्या किमतीच्या चार पट आहे!
इतिहास शोधणे
१८६९ मध्ये, मेंडेलीव्हने कॅल्शियम (४०) आणि टायटॅनियम (४८) मधील अणुवस्तुमानातील अंतर लक्षात घेतले आणि येथे एक न सापडलेला मध्यवर्ती अणुवस्तुमान घटक असल्याचे भाकीत केले. त्याने भाकीत केले की त्याचे ऑक्साईड X ₂ O Å आहे. १८७९ मध्ये स्वीडनमधील उप्साला विद्यापीठातील लार्स फ्रेडरिक निल्सन यांनी स्कॅन्डियमचा शोध लावला. त्याने ते काळ्या दुर्मिळ सोन्याच्या खाणीतून काढले, एक जटिल धातू ज्यामध्ये ८ प्रकारचे धातू ऑक्साईड असतात. त्याने ते काढले आहेएर्बियम(III) ऑक्साईडकाळ्या दुर्मिळ सोन्याच्या धातूपासून, आणि मिळवलेयटरबियम(III) ऑक्साईडया ऑक्साईडपासून, आणि हलक्या मूलद्रव्याचा आणखी एक ऑक्साईड मिळतो, ज्याचा वर्णपट दर्शवितो की तो एक अज्ञात धातू आहे. हा मेंडेलीव्हने भाकित केलेला धातू आहे, ज्याचा ऑक्साईडस्कॉओ₃. स्कॅन्डियम धातू स्वतःच तयार केला गेला होतास्कॅन्डियम क्लोराईड१९३७ मध्ये इलेक्ट्रोलाइटिक वितळण्याद्वारे.
मेंडेलीव्ह
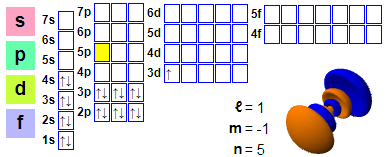
इलेक्ट्रॉन कॉन्फिगरेशन
इलेक्ट्रॉन कॉन्फिगरेशन: १s२ २s२ २p६ ३s२ ३p६ ४s२ ३d१
स्कॅन्डियम हा एक मऊ, चांदीचा पांढरा संक्रमण धातू आहे ज्याचा वितळण्याचा बिंदू १५४१ ℃ आणि उत्कलन बिंदू २८३१ ℃ आहे.
त्याच्या शोधानंतर बराच काळ, उत्पादनात अडचण आल्यामुळे स्कॅन्डियमचा वापर सिद्ध झाला नाही. दुर्मिळ पृथ्वी घटक पृथक्करण पद्धतींमध्ये वाढत्या सुधारणांसह, आता स्कॅन्डियम संयुगे शुद्ध करण्यासाठी एक परिपक्व प्रक्रिया प्रवाह आहे. स्कॅन्डियम हे यट्रियम आणि लॅन्थॅनाइडपेक्षा कमी अल्कधर्मी असल्याने, हायड्रॉक्साइड सर्वात कमकुवत आहे, म्हणून स्कॅन्डियम असलेले दुर्मिळ पृथ्वी घटक मिश्रित खनिज "स्टेप वर्षाव" पद्धतीने दुर्मिळ पृथ्वी घटकापासून वेगळे केले जाईल जेव्हा स्कॅन्डियम(III) हायड्रॉक्साइड द्रावणात हस्तांतरित केल्यानंतर अमोनियाने प्रक्रिया केली जाते. दुसरी पद्धत म्हणजे नायट्रेटच्या ध्रुवीय विघटनाद्वारे स्कॅन्डियम नायट्रेट वेगळे करणे. स्कॅन्डियम नायट्रेट विघटन करणे सर्वात सोपे असल्याने, स्कॅन्डियम वेगळे केले जाऊ शकते. याव्यतिरिक्त, युरेनियम, थोरियम, टंगस्टन, टिन आणि इतर खनिज साठ्यांमधून सोबत असलेल्या स्कॅन्डियमची व्यापक पुनर्प्राप्ती देखील स्कॅन्डियमचा एक महत्त्वाचा स्रोत आहे.
शुद्ध स्कॅन्डियम संयुग मिळवल्यानंतर, ते ScCl Å मध्ये रूपांतरित होते आणि KCl आणि LiCl सह वितळते. वितळलेल्या जस्तचा वापर इलेक्ट्रोलिसिससाठी कॅथोड म्हणून केला जातो, ज्यामुळे स्कॅन्डियम झिंक इलेक्ट्रोडवर अवक्षेपित होतो. नंतर, झिंकचे बाष्पीभवन करून धातूचे स्कॅन्डियम मिळते. हा एक हलका चांदीचा पांढरा धातू आहे जो अतिशय सक्रिय रासायनिक गुणधर्मांसह आहे, जो गरम पाण्याशी प्रतिक्रिया देऊन हायड्रोजन वायू तयार करू शकतो. म्हणून चित्रात तुम्हाला दिसणारा धातू स्कॅन्डियम एका बाटलीत बंद केला जातो आणि आर्गॉन वायूने संरक्षित केला जातो, अन्यथा स्कॅन्डियम त्वरीत गडद पिवळा किंवा राखाडी ऑक्साईड थर तयार करेल, त्याची चमकदार धातूची चमक गमावेल.
अर्ज
प्रकाश उद्योग
स्कॅन्डियमचे उपयोग अतिशय तेजस्वी दिशेने केंद्रित आहेत आणि त्याला प्रकाशाचा पुत्र म्हणणे अतिशयोक्तीपूर्ण नाही. स्कॅन्डियमचे पहिले जादूचे शस्त्र म्हणजे स्कॅन्डियम सोडियम दिवा, ज्याचा वापर हजारो घरांमध्ये प्रकाश आणण्यासाठी केला जाऊ शकतो. हा एक धातूचा हॅलाइड आहे विद्युत प्रकाश: बल्ब सोडियम आयोडाइड आणि स्कॅन्डियम ट्रायओडाइडने भरलेला असतो आणि त्याच वेळी स्कॅन्डियम आणि सोडियम फॉइल जोडले जातात. उच्च-व्होल्टेज डिस्चार्ज दरम्यान, स्कॅन्डियम आयन आणि सोडियम आयन अनुक्रमे त्यांच्या वैशिष्ट्यपूर्ण उत्सर्जन तरंगलांबींचा प्रकाश उत्सर्जित करतात. सोडियमच्या वर्णक्रमीय रेषा 589.0 आणि 589.6 एनएम आहेत, दोन प्रसिद्ध पिवळे दिवे आहेत, तर स्कॅन्डियमच्या वर्णक्रमीय रेषा 361.3~424.7 एनएम आहेत, जवळच्या अल्ट्राव्हायोलेट आणि निळ्या प्रकाश उत्सर्जनाची मालिका. कारण ते एकमेकांना पूरक असतात, त्यामुळे तयार होणारा एकूण प्रकाश रंग पांढरा प्रकाश असतो. स्कॅन्डियम सोडियम दिव्यांमध्ये उच्च प्रकाशमान कार्यक्षमता, चांगला प्रकाश रंग, वीज बचत, दीर्घ सेवा आयुष्य आणि मजबूत धुके तोडण्याची क्षमता ही वैशिष्ट्ये असल्याने ते टेलिव्हिजन कॅमेरे, चौक, क्रीडा स्थळे आणि रस्त्यावरील प्रकाशयोजनांसाठी मोठ्या प्रमाणावर वापरले जाऊ शकतात आणि तिसऱ्या पिढीतील प्रकाश स्रोत म्हणून ओळखले जातात. चीनमध्ये, या प्रकारच्या दिव्याला हळूहळू एक नवीन तंत्रज्ञान म्हणून प्रोत्साहन दिले जात आहे, तर काही विकसित देशांमध्ये, या प्रकारच्या दिव्याचा वापर १९८० च्या दशकाच्या सुरुवातीला मोठ्या प्रमाणावर केला जात होता.
स्कॅन्डियमचे दुसरे जादूचे शस्त्र म्हणजे सौर फोटोव्होल्टेइक पेशी, जे जमिनीवर पसरलेला प्रकाश गोळा करू शकतात आणि मानवी समाजाला चालना देण्यासाठी त्याचे विजेमध्ये रूपांतर करू शकतात. मेटल इन्सुलेटर सेमीकंडक्टर सिलिकॉन सोलर सेल आणि सोलर सेलमध्ये स्कॅन्डियम हा सर्वोत्तम अडथळा धातू आहे.
त्याचे तिसरे जादूचे शस्त्र γ किरण स्रोत असे म्हणतात. हे जादूचे शस्त्र स्वतःहून तेजस्वीपणे चमकू शकते, परंतु या प्रकारचा प्रकाश उघड्या डोळ्यांनी मिळू शकत नाही, हा एक उच्च-ऊर्जा फोटॉन प्रवाह आहे. आपण सहसा खनिजांमधून 45Sc काढतो, जे स्कॅन्डियमचे एकमेव नैसर्गिक समस्थानिक आहे. प्रत्येक 45Sc केंद्रकात 21 प्रोटॉन आणि 24 न्यूट्रॉन असतात. 46Sc, एक कृत्रिम किरणोत्सर्गी समस्थानिक, γ रेडिएशन स्रोत म्हणून वापरला जाऊ शकतो किंवा ट्रेसर अणूंचा वापर घातक ट्यूमरच्या रेडिओथेरपीसाठी देखील केला जाऊ शकतो. यट्रियम गॅलियम स्कॅन्डियम गार्नेट लेसरसारखे अनुप्रयोग देखील आहेत,स्कॅन्डियम फ्लोराईडटेलिव्हिजनवर काचेच्या इन्फ्रारेड ऑप्टिकल फायबर आणि स्कॅन्डियम लेपित कॅथोड रे ट्यूब. असे दिसते की स्कॅन्डियम ब्राइटनेससह जन्माला येतो.
मिश्रधातू उद्योग
अॅल्युमिनियम मिश्रधातूंच्या डोपिंगसाठी त्याच्या मूलभूत स्वरूपात स्कॅन्डियमचा मोठ्या प्रमाणावर वापर केला जात आहे. जोपर्यंत काही हजारवा भाग स्कॅन्डियम अॅल्युमिनियममध्ये जोडला जातो तोपर्यंत एक नवीन Al3Sc टप्पा तयार होईल, जो अॅल्युमिनियम मिश्रधातूमध्ये मेटामॉर्फिझमची भूमिका बजावेल आणि मिश्रधातूची रचना आणि गुणधर्म लक्षणीयरीत्या बदलतील. 0.2%~0.4% Sc (जे घरी तळलेल्या भाज्या ढवळण्यासाठी मीठ घालण्याच्या प्रमाणात खरोखर समान आहे, फक्त थोडेसे आवश्यक आहे) जोडल्याने मिश्रधातूचे पुनर्स्फटिकीकरण तापमान 150-200 ℃ ने वाढू शकते आणि उच्च-तापमान शक्ती, संरचनात्मक स्थिरता, वेल्डिंग कार्यक्षमता आणि गंज प्रतिकार लक्षणीयरीत्या सुधारू शकते. उच्च तापमानात दीर्घकालीन काम करताना सहजपणे होणारी भंगार घटना देखील टाळता येते. उच्च शक्ती आणि उच्च कडकपणा असलेले अॅल्युमिनियम मिश्र धातु, नवीन उच्च-शक्तीचे गंज-प्रतिरोधक वेल्डेबल अॅल्युमिनियम मिश्र धातु, नवीन उच्च-तापमान अॅल्युमिनियम मिश्र धातु, उच्च-शक्तीचे न्यूट्रॉन विकिरण प्रतिरोधक अॅल्युमिनियम मिश्र धातु, इत्यादी, एरोस्पेस, विमानचालन, जहाजे, अणुभट्ट्या, हलकी वाहने आणि हाय-स्पीड ट्रेन्समध्ये विकासाच्या अतिशय आकर्षक संधी आहेत.
स्कॅन्डियम हे लोखंडासाठी एक उत्कृष्ट मॉडिफायर देखील आहे आणि थोड्या प्रमाणात स्कॅन्डियम कास्ट आयर्नची ताकद आणि कडकपणा लक्षणीयरीत्या सुधारू शकते. याव्यतिरिक्त, स्कॅन्डियमचा वापर उच्च-तापमानाच्या टंगस्टन आणि क्रोमियम मिश्रधातूंसाठी एक मिश्रित पदार्थ म्हणून देखील केला जाऊ शकतो. अर्थात, इतरांसाठी लग्नाचे कपडे बनवण्याव्यतिरिक्त, स्कॅन्डियमचा वितळण्याचा बिंदू उच्च असतो आणि त्याची घनता अॅल्युमिनियमसारखीच असते आणि स्कॅन्डियम टायटॅनियम मिश्रधातू आणि स्कॅन्डियम मॅग्नेशियम मिश्रधातू सारख्या उच्च वितळण्याच्या बिंदूच्या हलक्या मिश्रधातूंमध्ये देखील वापरली जाते. तथापि, त्याच्या उच्च किंमतीमुळे, ते सामान्यतः फक्त स्पेस शटल आणि रॉकेट सारख्या उच्च-स्तरीय उत्पादन उद्योगांमध्ये वापरले जाते.
सिरेमिक मटेरियल
स्कॅन्डियम, एकच पदार्थ, सामान्यतः मिश्रधातूंमध्ये वापरला जातो आणि त्याचे ऑक्साइड सिरेमिक पदार्थांमध्ये त्याच प्रकारे महत्त्वाची भूमिका बजावतात. घन ऑक्साईड इंधन पेशींसाठी इलेक्ट्रोड पदार्थ म्हणून वापरता येणारे चतुष्कोणीय झिरकोनिया सिरेमिक पदार्थ, एक अद्वितीय गुणधर्म आहे जिथे वातावरणात वाढत्या तापमान आणि ऑक्सिजन एकाग्रतेसह या इलेक्ट्रोलाइटची चालकता वाढते. तथापि, या सिरेमिक पदार्थाची क्रिस्टल रचना स्वतः स्थिरपणे अस्तित्वात राहू शकत नाही आणि त्याचे कोणतेही औद्योगिक मूल्य नाही; त्याचे मूळ गुणधर्म राखण्यासाठी ही रचना निश्चित करू शकणार्या काही पदार्थांचे डोपिंग करणे आवश्यक आहे. 6~10% स्कॅन्डियम ऑक्साईड जोडणे हे एका काँक्रीटच्या रचनेसारखे आहे, जेणेकरून झिरकोनिया चौकोनी जाळीवर स्थिर करता येईल.
डेन्सिफायर आणि स्टेबिलायझर्स म्हणून उच्च-शक्ती आणि उच्च-तापमान प्रतिरोधक सिलिकॉन नायट्राइड सारखे अभियांत्रिकी सिरेमिक साहित्य देखील आहेत.
घनता वाढवणारा म्हणून,स्कॅन्डियम ऑक्साईडसूक्ष्म कणांच्या काठावर एक रेफ्रेक्ट्री फेज Sc2Si2O7 तयार करू शकते, ज्यामुळे अभियांत्रिकी सिरेमिकचे उच्च-तापमान विकृतीकरण कमी होते. इतर ऑक्साईड्सच्या तुलनेत, ते सिलिकॉन नायट्राइडचे उच्च-तापमान यांत्रिक गुणधर्म अधिक चांगल्या प्रकारे सुधारू शकते.
उत्प्रेरक रसायनशास्त्र
रासायनिक अभियांत्रिकीमध्ये, स्कॅन्डियमचा वापर अनेकदा उत्प्रेरक म्हणून केला जातो, तर Sc2O3 चा वापर इथेनॉल किंवा आयसोप्रोपॅनॉलचे निर्जलीकरण आणि डीऑक्सिडेशन, एसिटिक ऍसिडचे विघटन आणि CO आणि H2 पासून इथिलीनचे उत्पादन यासाठी केला जाऊ शकतो. Sc2O3 असलेले Pt Al उत्प्रेरक पेट्रोकेमिकल उद्योगात जड तेल हायड्रोजनेशन शुद्धीकरण आणि शुद्धीकरण प्रक्रियेसाठी देखील एक महत्त्वाचे उत्प्रेरक आहे. क्युमिनसारख्या उत्प्रेरक क्रॅकिंग अभिक्रियांमध्ये, Sc-Y झिओलाइट उत्प्रेरकाची क्रिया अॅल्युमिनियम सिलिकेट उत्प्रेरकापेक्षा 1000 पट जास्त असते; काही पारंपारिक उत्प्रेरकांच्या तुलनेत, स्कॅन्डियम उत्प्रेरकांच्या विकासाच्या शक्यता खूप उज्ज्वल असतील.
अणुऊर्जा उद्योग
उच्च-तापमान अणुभट्टी अणुइंधनात UO2 मध्ये थोड्या प्रमाणात Sc2O3 जोडल्याने UO2 ते U3O8 रूपांतरणामुळे होणारे जाळीचे रूपांतर, आकारमान वाढ आणि क्रॅकिंग टाळता येते.
इंधन सेल
त्याचप्रमाणे, निकेल अल्कली बॅटरीमध्ये २.५% ते २५% स्कॅन्डियम जोडल्याने त्यांचे आयुष्य वाढेल.
कृषी प्रजनन
शेतीमध्ये, कॉर्न, बीट, वाटाणा, गहू आणि सूर्यफूल यांसारख्या बियाण्यांवर स्कॅन्डियम सल्फेटचा उपचार केला जाऊ शकतो (साधारणपणे त्याची एकाग्रता १०-३~१०-८ मोल/लिटर असते, वेगवेगळ्या वनस्पतींमध्ये वेगवेगळी असते), आणि उगवण वाढवण्याचा प्रत्यक्ष परिणाम साध्य झाला आहे. ८ तासांनंतर, रोपांच्या तुलनेत मुळांचे आणि कळ्यांचे कोरडे वजन अनुक्रमे ३७% आणि ७८% वाढले, परंतु या यंत्रणेचा अजूनही अभ्यास सुरू आहे.
अणु द्रव्यमान डेटाच्या कर्जाकडे निल्सनने लक्ष दिल्यापासून ते आजपर्यंत, स्कॅन्डियम लोकांच्या दृष्टीत फक्त शंभर किंवा वीस वर्षे प्रवेश केला आहे, परंतु तो जवळजवळ शंभर वर्षे बेंचवर बसला आहे. गेल्या शतकाच्या उत्तरार्धात भौतिक विज्ञानाच्या जोरदार विकासानंतरच त्याला चैतन्य मिळाले. आज, स्कॅन्डियमसह दुर्मिळ पृथ्वी घटक, भौतिक विज्ञानात गरम तारे बनले आहेत, हजारो प्रणालींमध्ये सतत बदलणारी भूमिका बजावत आहेत, दररोज आपल्या जीवनात अधिक सोयीस्करता आणत आहेत आणि मोजणे आणखी कठीण असलेले आर्थिक मूल्य निर्माण करत आहेत.
पोस्ट वेळ: जून-२९-२०२३